Урок предназначается для
самостоятельного прохождения темы «Ароматические углеводороды. Химические
свойства». В ходе этого занятия вы сможете расширить свои знания об
ароматических углеводородах, узнаете о том, какими химическими свойствами
обладает этот класс соединений.
Бензол – это стабильная
высокосимметричная молекула, обладающая избытком электронной плотности.
Разорвать p-электронное облако в молекуле бензола сложно. Поэтому бензол
вступает в химические реакции значительно менее активно по сравнению с
непредельными соединениями.
Наиболее характерными
являются реакции электрофильного замещения. Например, галогенирование,
нитрование, сульфирование и алкилирование. В реакции галогенирования ни
фторирование, ни йодирование не используется, так как фтор слишком активен, а йод
не активен, и реакция с ним не идет.
2. Механизм реакции
галогенирования
Необходим катализатор
(бромид железа (III) или алюминия) и недопустимо попадание даже небольших
количеств воды. Роль катализатора заключается в том, что молекула брома
притягивается одним из атомов брома к атому железа. В результате она
поляризуется – пара электронов связи переходит к атому брома, связанному с
железом:
Br+….Br–FeBr3
Br+ – сильный электрофил.
Он притягивается к шестиэлектронному облаку бензольного кольца и разрывает его,
образуя ковалентную связь с атомом углерода:
К образовавшемуся катиону
мог бы присоединиться анион брома. Но восстановление ароматической системы
бензольного кольца энергетически более выгодно, чем присоединение аниона брома.
Поэтому молекула переходит в стабильное состояние, высвободив ион водорода:
По аналогичному механизму
протекают все реакции электрофильного замещения в бензольном кольце.
3. Нитрование
В реакции нитрования в
качестве катализатора используется серная кислота.
Бензол и его гомологи
взаимодействуют со смесью концентрированных серной и азотной кислот (нитрующей
смесью). В нитрующей смеси в равновесии существует иона нитрония NO2+, который
является электрофилом:
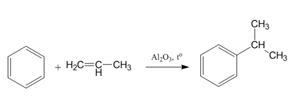
4. Алкилирование
Алкилирование алкенами
5. Сульфирование
Бензол и другие арены при
нагревании реагируют с концентрированной серной кислотой или олеумом –
раствором SO3 в серной кислоте:
Для бензола и его
гомологов существуют и реакции, не относящиеся к электрофильному замещению.
6. Реакции с разрушением
бензольного кольца
Эти реакции энергетически
невыгодны, поэтому протекают только при нагревании или облучении.
1. Гидрирование.
При нагревании,
повышенном давлении и в присутствии катализатора Ni, Pt или Pd бензол и другие
арены присоединяют водород, образуя циклогексан:
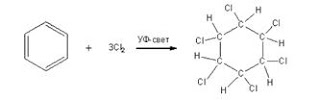
2. Хлорирование бензола
Под действием
ультрафиолетового излучения бензол присоединяет хлор. Если колбу из кварцевого
стекла с раствором хлора в бензоле вынести на солнечный свет, раствор быстро
обесцветится, хлор присоединится к бензолу с образованием
1,2,3,4,5,6-гексахлорциклогексана, который известен под названием гексахлоран
(ранее применялся как инсектицид):
3. Горение бензола
В отличие от алканов,
пламя у бензола и других ароматических углеводородов яркое, коптящее.
Подведение итога урока
На этом уроке вы изучили
тему «Химические свойства ароматических углеводородов». Используя этот
материал, вы смогли получить представление о химических свойствах бензола, а
также о жёстких условиях, которые необходимы для того, чтобы бензол вступил в
реакцию с другими веществами.










Комментариев нет:
Отправить комментарий